燃料的燃烧
一、燃烧的条件
1.根据经验我们知道,有的物质可以燃烧,如酒精、红磷、木炭等;有的物质不能燃烧,如水、大理石等。只有可燃物才能发生燃烧,________是燃烧发生的条件之一。
2.探究-燃烧的条件
【问题】
除了可燃物,燃烧还需要哪些条件呢?
【预测】
回忆红磷在氧气中燃烧的事实,通过分析反应的化学方程式,预测燃烧可能与哪些因素有关。
【实验步骤】
(1)在500 mL 烧杯中加入300 mL 热水,并放入用硬纸圈圈住的一小块白磷,在烧杯上盖一片薄铜片。在铜片的一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸去表面上水的白磷,观察实验现象。
(2)用导管对准上述烧杯热水中的白磷,通入少量氧气,观察实验现象。
【分析与结论】
(1)实验步骤(1)中铜片上白磷燃烧而红磷不燃烧的事实,说明燃烧需要什么条件。
(2)实验步骤(1)中铜片上白磷燃烧而热水中白磷不燃烧的事实,说明燃烧还需要什么条件。
(3)实验步骤(2)中向热水中通入氧气(或空气)后白磷燃烧的事实, 再次说明燃烧需要什么条件。
(4)综合上述分析,请你尝试总结燃烧需要哪些条件。
3.燃烧:通常情况下_________与_________发生的一种________________________________。
4.燃烧所需要的条件(三个条件必须同时满足)
(1)____________________________________。
(2)____________________________________。
(3)____________________________________。
二、燃料燃烧的调控
1.燃料的充分燃烧
【思考与讨论】
在日常生活中你是否遇到这样的情况:做饭时,有时燃气灶的火焰呈现黄色或橙色,锅底出现黑色物质。此时就需要调节一下灶具的进风口,这是为什么呢?
(1)当________不充足时,燃料不能充分燃烧,产生黑烟,并生成_______________等物质,使燃料的利用率降低,浪费资源,且污染空气。
(2)使燃料充分燃烧,通常要考虑:燃烧时要有足够的______________ ,燃料与空气要有足够大的_________________。
2.灭火的原理和方法
【思考与讨论】
①下面是一些防火和灭火的措施,试分析其应用的原理。
炒菜时油锅中的油不慎着火,可用锅盖盖灭或放入较多的蔬菜;
堆放杂物的纸箱着火时,可用水浇灭;
油罐着火时需用水喷淋,使罐体降温;
在森林中或森林与村庄之间设置防火隔离带。
②根据燃烧的条件及以上事实,请你归纳灭火的原理。
(1)灭火原理:通过分析我们知道,________或________________,________(或________) ,以及________________,都能达到灭火的目的。所以说,灭火的原理就是要________________。
(2)探究-简易灭火器的设计与制作
【问题】
通常使用的灭火器的原理是什么?如何设计与制作简易灭火器?
【实验与分析】
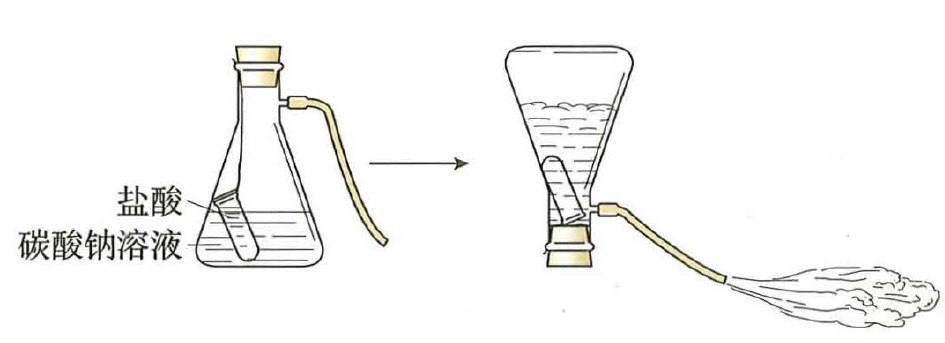
点燃三支蜡烛,在其中一支蜡烛上扣一个烧杯;将另两支蜡烛分别放在两个烧杯中;然后向一个烧杯中加适量碳酸钠溶液和盐酸。蜡烛燃烧的现象有什么不同?请用灭火的原理分析和解释。

【设计与制作】
根据灭火原理及上述实验Ⅲ所利用的化学反应原理,可以设计一种简易灭火器。
(3)灭火器及其灭火原理和适用范围
①干粉灭火器:除可用来扑灭一般火灾外,还可用来扑灭______、______等燃烧引起的失火。
②二氧化碳灭火器:扑灭______、______、______和______等物的失火
③水基型灭火器:扑灭非水溶性可燃液体,如______、______,以及固体材料,如______、______等燃烧引起的失火
(4)如果发现火险或遭遇火灾,一定不要慌张,要沉着应对,并立即拨打______火警电话。如果火势不大,可根据可燃物及起火原因等现场情况,选择合适的方法和____________将火扑灭;如果火势较大或有蔓延的趋势和可能,应采取必要的自救措施,如采用____________等方式迅速离开着火区域。
3.易燃物和易爆物的安全知识
(1)爆炸:可燃物在__________内__________地燃烧,就会在短时间内__________,使__________而引起爆炸。
(2)爆炸极限:可燃气体等在空气中达到一定的含量时,遇到火 源就会发生爆炸,____________________,叫做爆炸极限。
三、化学反应中的能量变化
1.酒精是_________(C2H5OH)的俗称,在空气中燃烧,发生化学反应时放出大量的热量。化学方程式:____________________。
2.【实验7-1】
在一支试管中加入一小匙干燥的生石灰(CaO) 或一小块生活中使用的生石灰干燥剂,插入温度计,再加入约2mL 水。观察现象。
(1)现象:__________________;
(2)化学方程式:__________________。
3.化学反应在生成___________的同时,还伴随着___________的变化,化学反应中的能量变化通常表现为___________的变化。有些反应放出热量,而有些反应则是吸收热量的,化学不仅研究______变化,还研究物质变化过程中伴随的______变化。
必记知识点
一、燃烧的定义
通常情况下,可燃物与氧气发生的一种发光、放热的剧烈的氧化反应叫做燃烧
二、燃烧的条件
1.探究-燃烧的条件
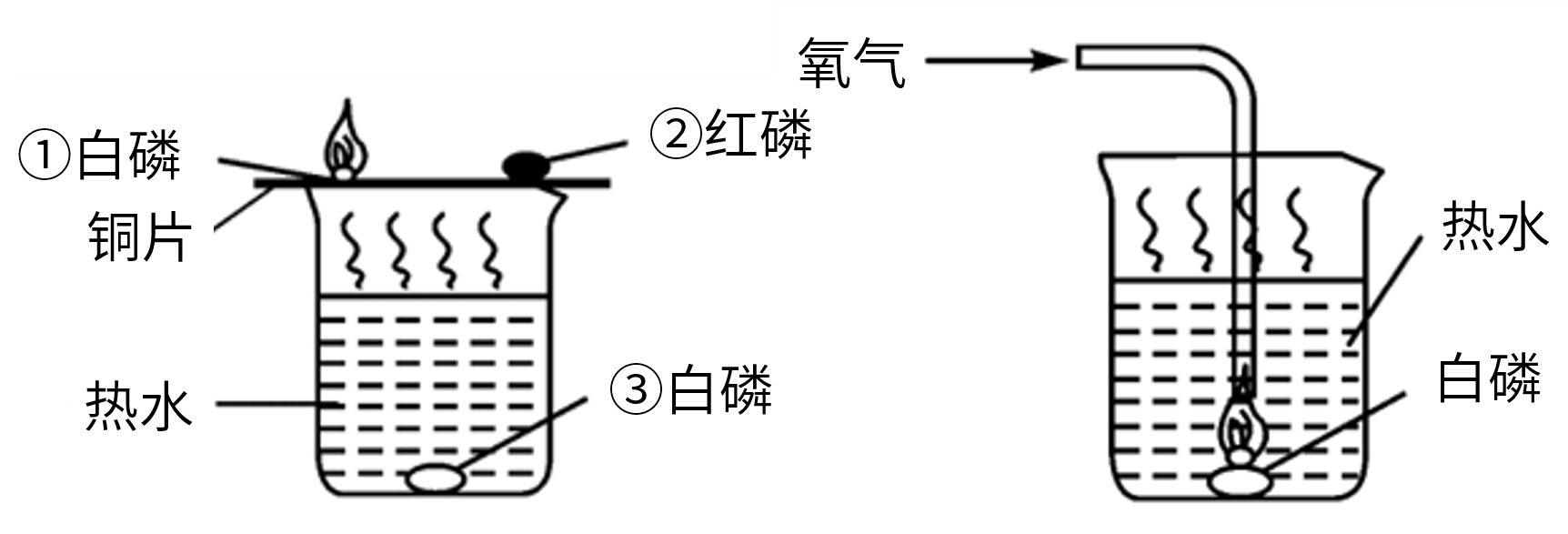
现象:铜片上的白磷燃烧;铜片上的红磷不燃烧(温度未到达着火点);热水中的白磷不燃烧(未与氧气或空气接触);通入氧气后热水中的白磷燃烧
分析:①②对比,燃烧需要温度达到着火点
①③对比,燃烧需要与氧气(或空气)接触
通入氧气前后对比,燃烧需要与氧气(或空气)接触
2.燃烧的条件
①可燃物
②与氧气(或空气)接触
③温度达到着火点
注意:燃烧的三个条件缺一不可
三、灭火原理
1.燃烧与灭火是里两个相反的过程,灭火的原理即破坏燃烧的条件
2.灭火的原理
①清除可燃物
②隔绝氧气(或空气)
③使温度降低到着火点以下
3.灭火器的适用范围
①泡沫灭火器:木材、棉布等引起的火灾
②干粉灭火器:油、气等引起的一般火灾
③二氧化碳灭火器:图书、档案、精密仪器等引起的火灾
四、易燃物和易爆物的安全知识
爆炸:可燃物在有限的空间内急剧地燃烧,就会在短时间内聚积大量的热,使气体的体积迅速膨胀而引起爆炸。
爆炸极限:可燃性气体等在空气中达到一定的含量时,遇到火源就会发生爆炸。
五、燃料的充分燃烧
1.燃烧时要有足够的空气(氧气)
2.燃料与空气(氧气)要有足够大的接触面积
六、化学反应中的能量变化
1.放热反应
(1)乙醇(C2H5OH),俗称酒精,燃烧时会放出大量的热
(2)氧化钙(生石灰)与水反应生成氢氧化钙(熟石灰),并放出热量
2.吸热反应
(1)碳还原二氧化碳