我们周围的空气
一、空气的组成
1.拉瓦锡实验
(1)实验药品______,反应后生成物的颜色和状态______; (2)拉瓦锡通过这个实验得出了空气由______和______组成的,其中氧气约占空气总体积的______。
2.测定空气中氧气含量的实验
(1)操作:在集气瓶内加入少量水,将水面上方空间分为5等份,并做好标记。用弹簧夹夹紧乳胶管。在燃烧匙内放入足实验量的红磷,用酒精灯加热,点燃红磷后立即伸入瓶中并把橡胶塞塞紧。待红磷熄灭并冷却至室温,打开弹簧夹。
(2)原理:红磷在空气中燃烧,消耗掉封闭容器内空气中的______,且______(填“有”或“没有”)产生新的气体,使容器内的压强______(填“增大”或“减小”),冷却后打开弹簧夹,烧杯内的水会被压入集气瓶,进入水的体积即为瓶内消耗______的体积。
(3)现象:红磷燃烧产生大量____________,并放出热量,冷却后打开弹簧夹,烧杯中的水__________________,瓶内液面上升约______。
(4)结论:氧气约占空气体积的______。
【思考】
①为什么红磷需要足量?
②实验时,通常会事先在集气瓶内装一部分水其作用是什么?
③为什么要等装置冷却后再打开止水夹?
④实验结束后瓶中剩余气体是什么?根据上述实验,红磷熄灭了,说明氮 气能不能支持燃烧?集气瓶内液面上升到一定高度后,还能继续上升吗?这种现象能不能说明氮气不易溶于水?
⑤为什么点燃红磷后要立即伸入瓶中,如果缓慢伸入会有什么影响?
3.空气的组成
按______计算:______占78%,______占21%,______占0.94%,______占0.03%,______占0.03%。
4.物质分类(混合物与纯净物)
(1)混合物是由____________混合而成的物质,组成混合物的各种成分的性质______。如________________________。
(2)纯净物是由__________________组成,如________________________,纯净物可以用____________来表示。
二、空气是一种宝贵的资源
1.氧气(O2)
(1)可______,常用于__________________等。
(2)可______,常用于__________________等。
2.氮气(N2)
(1)______色______味的______体,______溶于水。
(2)不能燃烧,也不支持燃烧。
(3)氮气的化学性质______,因此常用作______。焊接金属时常用氮气做______;食品包装时充入N2以______。
(4)液氮温度______,医疗上可利用液氮进行____________,超导材料在液氮的______环境下能显示超导性能。
(5)N2是制造______和______的重要原料。
3.稀有气体
(1)稀有气体包括______、______、______、氪、氙和氡。它们都是______颜色,______气味的气体,化学性质____________。
(2)稀有气体在通电时能发出____________,可作____________,如______、______、______、______。液态氦可用于制造______,氦气密度______,可用于制作____________。
三、保护大气环境
1.空气的污染物有排放到空气中的______和______。
2.空气污染的危害
(1)严重损害____________,影响____________,破坏____________;
(2)臭氧层破坏和______等。
3.保护空气的措施
(1)使用清洁能源;
(2)加强____________;
(3)积极____________、种草等。
4.目前计入空气质量评价的主要污染物为______、______、______、可吸入颗粒物(PM10)、细颗粒物(PM2.5)和______等。二氧化碳______(填“属于”或“不属于”)空气污染物。
5.空气质量日报中,空气质量指数的数值越大,空气质量越______。
必记知识点
一、空气中氧气含量的测定
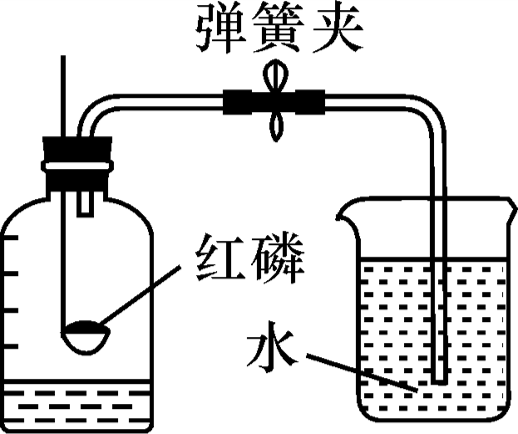
1.实验原理
红磷燃烧,消耗空气的中的氧气,使集气瓶内压强降低,在大气压的作用下将烧杯内的水压入集气瓶,进入水的体积等于消耗氧气的体积
2.文字表达式
3.实验步骤
①检查装置气密性
②在集气瓶中装少量水,再把水以上的容积部分分成五等份做上记号
③点燃燃烧匙中的红磷,立即伸入瓶内并塞紧瓶塞
④待红磷燃烧停止,温度降低到室温后打开弹簧夹
4.实验现象
放热、产生大量白烟
冷却至室温,打开弹簧夹,烧杯中的水进入集气瓶,水的体积约占瓶内空气体积的1/5
5.实验结论
空气中氧气的体积约占空气体积的1/5
6.误差分析
(1)小于1/5
装置漏气
红磷的量不足
未冷却到室温就打开弹簧夹
部分水留在导管中,未进入集气瓶
(2)大于1/5
弹簧夹没有夹紧,红磷燃烧时集气瓶内受热气体会顺着导管逸出
燃烧匙伸入过慢,使装置内气体受热逸出
7.选择红磷的原因
能与空气中的氧气反应,不与空气中其他成分反应
反应后生成物不是气体(不能选择硫、木炭代替红磷)
二、空气的成分(体积分数)
氮气:78%;氧气:21%稀有气体(氦、氖、氩、氪、氙、氡):0.94%;二氧化碳:0.03%;其他气体和杂质:0.03%
三、物质分类
1.混合物:两种或两种以上物质混合而成的物质(不能用化学符号)
例:空气、海水、纯净水
2.纯净物:一种物质组成的物质(可以用化学符号表示)
例:氧气、氮气、二氧化碳、冰水混合物
四、空气是一种宝贵的资源
1.氧气
供给呼吸(动植物呼吸、医疗急救)
支持燃烧(炼钢、气割、气焊、航空航天)
2.氮气
(1)性质
①无色、无味、气体,不易溶于水
③不能燃烧、也不支持燃烧(化学性质不活泼)
(2)用途
制硝酸、氮肥的重要原料
保护气(焊接金属、食品包装)
液氮冷冻麻醉
3.稀有气体(惰性气体)
(1)性质
①无色无味的气体
②化学性质很不活泼
(2) 用途
作保护气;作电光源;氦气制造低温环境
五、保护空气
1.污染物
有害气体:二氧化硫、二氧化氮、一氧化碳
烟尘:
2.危害
损害人体健康;影响作物生长;破坏生态平衡;臭氧层破坏;酸雨。
3.保护
使用清洁能源;加强空气质量监测;植树造林、种草