物质组成的表示
一、化学式
1.化学式的定义:用___________和___________的组合表示物质___________的式子。
2.每种纯净物的组成是___________的,所表示每种物质组成的化学式只有___________。
【思考与讨论】
符号H 、2H 、H2 、2H2各具有什么意义?
3.化学式的书写
(1)物质的组成是通过___________的,因此化学式的书写必须依据___________。
(2)当某组成元素原子个数是___________时,___________省略不写。
(3)书写氧化物的化学式时,一般把氧的元素符号写在___________,另一种元素的符号写在___________。如二氧化碳___________。(有氧在后)
(4)由金属与非金属组成的化合物,书写其化学式时,一般把金属的元素符号写在左边,非金属的元素符号写在右边。如氯化钠:___________。(金前非后)
(5)单质化学式的书写
①金属、固态非金属、稀有气体:直接用___________表示。(“金”、“石”、“稀”)
②气态非金属:元素符号+数字
4.化学式的读法
由两种元素组成的化合物的名称,一般读作___________,例如NaCl读作___________。有时还要读出化学式中各种元素的原子个数,例如CO2读作___________,Fe3O4读作___________。
5.化学式的意义
(1)化学式H2O的意义
宏观:______________________;______________________;
微观:______________________;______________________。
(2)2H2O的意义
微观:______________________
(3)Fe的意义
宏观:______________________;______________________;
微观:______________________;
(4)2Fe的意义
微观:______________________
二、化合价
1.化合价规律
(1)元素的化合价有_______、有_______,在化合物里,正、负化合价的代数和为_______ 。
(2)金属元素与非金属元素化合时,金属元素显_______价,非金属元素显_______价;
(3)一些元素在不同物质中可显_______的化合价;
(4)在单质里,元素的化合价为______。
2.原子团(根)
(1)一些带电荷的原子团,常作为一个整体参加反应,这样的原子团又叫做______,根也有化合价。
(2)带电的原子团也叫______。
(3)氢氧根离子:______,化合价为______;碳酸根离子:______,化合价为______;硫酸根离子:______,化合价为______;硝酸根离子:______,化合价为______;铵根离子:______,化合价为______。
3.化合价的应用
(1)会标化合价
化合价应写在元素符号的_______,例如标出氯化镁(MgCl2)中镁元素的化合价:_______。
(2)会算化合价(根据已知元素的化合价算未知元素的化合价)
①依据:化合物里元素正负化合价的代数和为_______。
②例子:计算并标出K2MnO4中锰元素的化合价。
已知钾元素的化合价为_______,氧元素的化合价为_______。
列式子:(+1)×___+( )×___+(-2)×___=0
所以K2MnO4中锰元素的化合价为_______。
(3)会根据化合价写化学式
【思考与讨论】
(1)在利用高锰酸钾制取氧气的反应中,有三种含锰元素的物质: KMn04 (高锰酸钾)、K2Mn04(锰酸钾)和Mn02(二氧化锰)。查化合价,尝试说出这三种物质中锰元素的化合价。
(2)写出溴化钠、氯化钙、氧化铝、二氧化氮的化学式。
三、物质组成的定量认识
1.计算相对分子质量
(1)相对分子质量是化学式中各原子的_______总和,符号为_______。
(2)物质相对分子质量=_____________________。
(3)练习:计算下列物质的相对分子质量
①CO2:_____________________
②CaCO3:_____________________
③Mg(OH)2:_____________________
2.计算物质组成元素的质量比
(1)物质组成元素的质量比= _____________________。
(2)练习:计算下列物质中各组成元素的质量比
①H2SO4:_____________________
②NH4NO3:_____________________
③(NH4)2SO4:_____________________
3.计算物质中某元素的质量分数
(1)物质中某元素的质量分数= _____________________。
(2)练习
①计算尿素【CO(NH)2】中氮元素的质量分数。
②计算硫酸中氧元素的质量分数。
③计算硝酸铵【 NH4NO3】中氮元素的质量分数。
必记知识点
一、化学式
1.化学式的定义
化学式:用元素符号和数字的组合表示物质组成的式子
混合物:无化学式
纯净物:唯一化学式
2.化学式的书写
(1)单质
金属、固态非金属、稀有气体(“金”、“石”、“稀”):直接用元素符号表示
气态非金属:元素符号+数字
(2)化合物
两种元素:金前非后(NaCl、MgCl2、KCl),有氧在后(CO2、Fe3O4、P2O5)
两种以上元素:KMnO4、K2MnO4
3.化学式的意义
宏观:表示某物质、某物质的元素组成
微观:表示1个分子、分子的原子构成
例:H2O
宏观:表示水;表示水由氢、氧两种元素组成
微观:表示1个水分子;表示1个水分子由2个氢原子和1个氧原子构成
例:2H2O
表示2个水分子
4.H、2H、H2、2H2的意义
H:氢元素、一个氢原子
2H:两个氢原子
H2:氢气、氢气由氢元素组成、1个氢分子、1个氢分子由两个氢原子构成
2H2:2个氢分子
5.化学式的读法
由两种元素组成的化合物的名称,一般读作某化某,有时还要读出化学式中各种元素的原子个数。
二、化合价
1.化合价:原子间相互化合的数目,元素化合价是元素的原子在形成化合物时表现出来的一种性质。
2.化合价一般规律
(1)化合价有正价、负价(正负在前,数字在后)
(2)同种元素在不同化合物中可显不同的化合价
(3)在化合物里正、负化合价的代数和为0
(4)单质中元素的化合价为0
(5)原子团(根):常作为一个整体参加反应的原子集团
铵根离子:NH4+;氢氧根离子:OH-;硝酸根离子:NO3-;碳酸根离子:CO32-;硫酸根离子:SO42-;
3.常见元素的化合价(口诀)
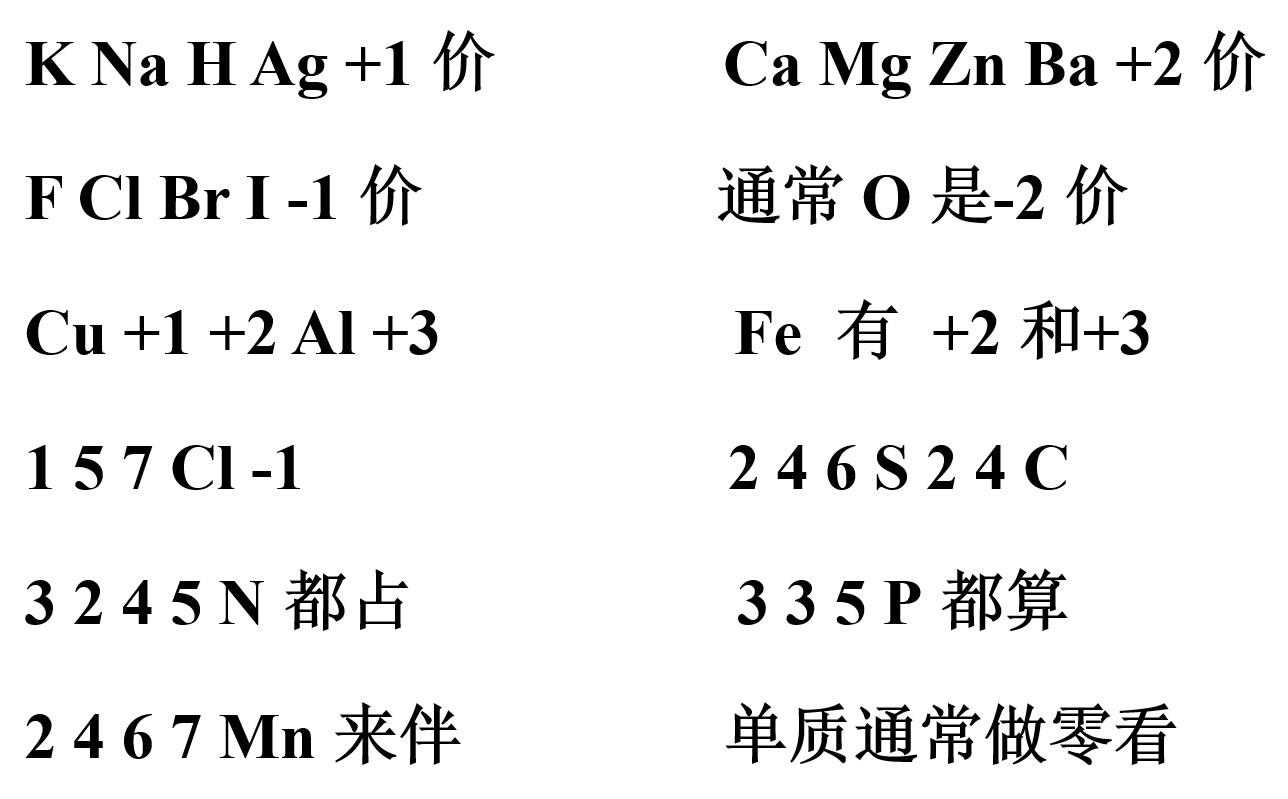
4.化合价的应用
(1)会标化合价
(2)会算化合价
(3)会根据化合价写化学式
三、有关相对分子质量的计算
1.会算相对分子质量
例:CO2的相对分子质量=12×1+16×2=44
2.会算物质组成元素的质量比
例:CO2中碳元素与氧元素的质量比=(12×1):(16×2)=3:8
3.会算物质中某元素的质量分数
CO2中碳元素的质量分数=×100%=27.3%