质量守恒定律
1.质量守恒定律:_______________________
2.判断下列说法是否正确:
(1)水变成水蒸气,质量不变,遵守质量守恒定律
(2)碳酸钠与稀盐酸反应后,测得质量减少,不遵守质量守恒定律
3.铜与氧气反应前后质量的测定:
(1)实验现象:_______物质逐渐变为_______,气球先_______后_______,m1_____(填“=”或“≠”)m2
(2)分析:参加反应的物质质量之和_____反应后生成的物质质量之和
4.铁与硫酸铜反应前后质量的测定:
(1)实验现象:铁钉表面有_______物质生成,溶液由_______变为_______,m1_____(填“=”或“≠”)m2
(2)分析:参加反应的物质质量之和_____反应后生成的物质质量之和
5.盐酸与碳酸钠反应前后质量的测定:
(1)实验现象:烧杯中产生_______,m1_____(填“=”或“≠”)m2
(2)m1>m2原因:_____________________
6.镁条燃烧前后质量的测定:
(1)实验现象:镁条燃烧,发出_______,产生大量_______,生成_______色固体,m1_____(填“=”或“≠”)m2
(2)m1<m2原因:_____________________
m1\>m2原因:\_\_\_\_\_\_\_\_\_\_\_\_\_\_\_\_\_\_\_\_\_
7.对于有气体参与或生成的反应,验证质量守恒定律,应在____________中进行
8.化学反应(化学变化)的实质:________________________
9.化学反应六不变:
宏观:________不变;元素________不变;元素________不变
微观:原子________不变,原子________不变;原子________不变
10.化学反应两改变:
宏观:________一定改变
微观:________一定改变
11.化学反应一可能改变:
________可能改变
12.化学方程式的意义:
(1)反应物、生成物、反应条件
(2)反应物、生成物各物质间质量比=________×________之比
(3)粒子个数比=________比
1-5单元化学方程式书写过关
1.碳燃烧:________________________
2.硫燃烧:________________________
3.红磷燃烧:________________________
4.铁丝燃烧:________________________
5.镁条燃烧:________________________
6.高锰酸钾制取氧气:________________________________
7.过氧化氢制取氧气:________________________________
8.汞和氧气反应:________________________________
9.氧化汞加热分解:________________________________
10.氢气燃烧:________________________________
11.电解水:________________________________
12.铜与氧气反应:________________________________
13.铁和硫酸铜溶液反应:________________________________
14.碳酸钠与稀盐酸反应:________________________________
15.氢氧化钠溶液和硫酸铜溶液反应:________________________________
16.高温煅烧大理石:________________________________
课外化学方程式的书写
1.肼-空气燃料电池有望应用于汽车工业,其原理是肼(N2H4)与氧气在特定条件下反应生成一种单质和水,该反应的化学方程式为:________________________________
2.工业制铝原理为电解熔融的Al2O3,生成铝和一种可供呼吸的气体。该反应的化学方程式为:________________________________
3.84消毒液中次氯酸钠自身没有消毒作用,有消毒作用的是次氯酸钠(NaClO)与空气中二氧化碳反应得到的次氯酸(HClO) ,反应中还产生碳酸钠,写出反应的化学方程式:________________________________
4.“洁厕灵(HCl)”与“84消毒液(NaClO)”不能混用。二者若混合,其有效成分之间能发生化学反应,产生氯化钠、水和有毒的氯气(Cl2),化学方程式为:________________________________
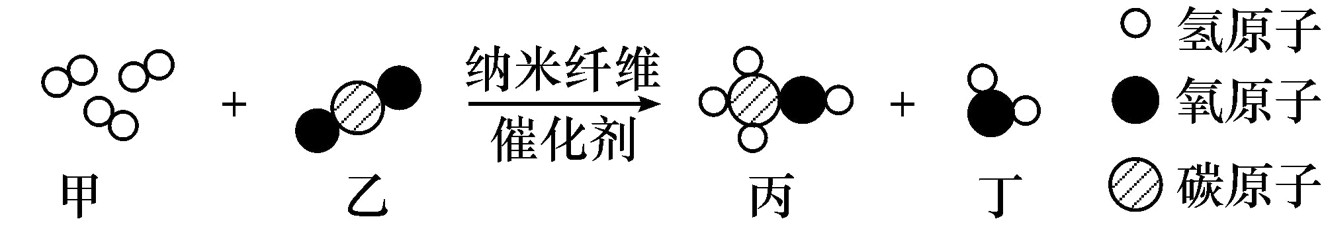
5.
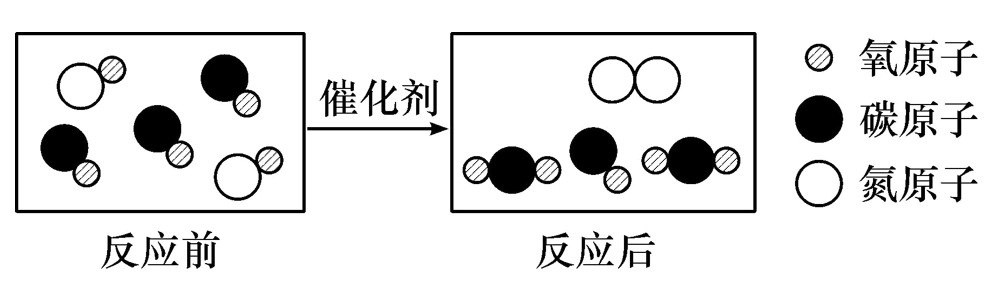
6.
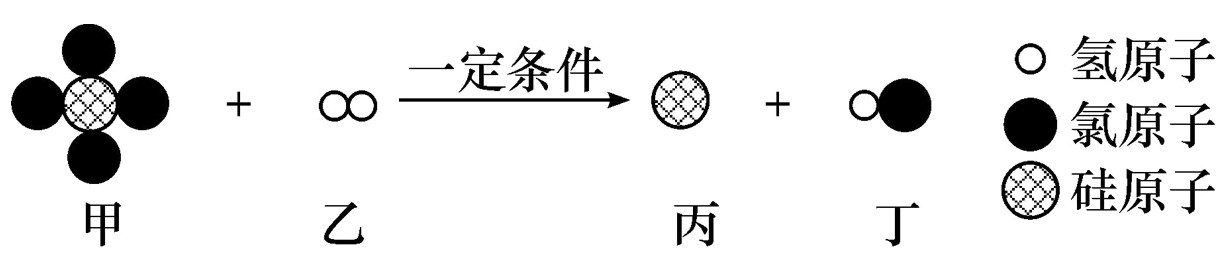
7.
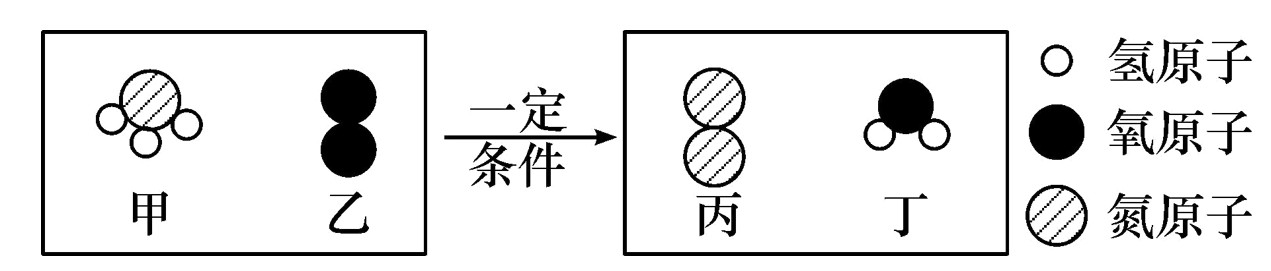
8.
9.
10.请按书写规范写出石油液化气中可燃物C3H8完全燃烧的化学方程式(提示:碳元素完全燃烧生成二氧化碳,氢元素完全燃烧生成水):________________________________________
11.铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],其受热分解生成三种氧化物,化学方程式为:________________________________________
12.汽车尾气(含有一氧化碳与一氧化氮等物质)是城市空气的污染源,治理的方法之一是在汽车的排气管上装一个催化转换器,使一氧化碳与一氧化氮反应生成氮气和二氧化碳。该反应的化学方程式为:________________________________________
13.NH3与氧气受热生成氮气和水,该反应的化学方程式为:________________________________________
14.安全气囊的起爆物质是叠氮化钠(NaN3)。叠氮化钠是一种白色固体,溶于液氨和水,微溶于乙醇。受到撞击时,叠氮化钠爆炸分解为金属钠和氮气。该反应的化学方程式为:________________________________________
15.可用氧化铁与过氧化钠(Na2O2)反应制取高铁酸钠(Na2FeO4),同时生成氧化钠,写出该反应的化学方程式:________________________________________