实验突破
二氧化碳的性质探究
一、倾倒二氧化碳
1.实验装置图
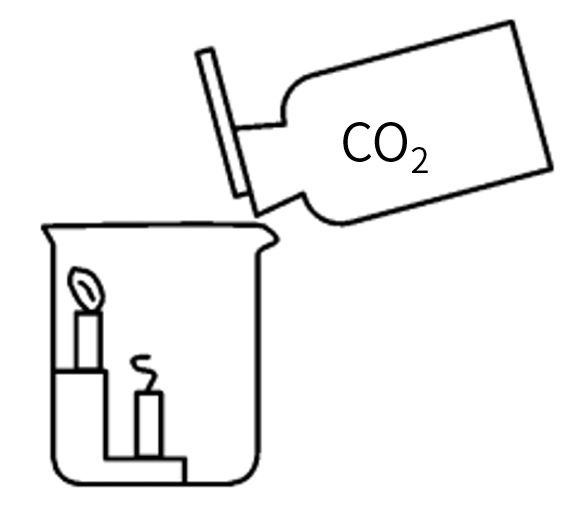
2.实验操作
将二氧化碳气体慢慢的倒入烧杯中,观察现象并分析
3.实验现象
蜡烛至下而上,依次熄灭
4.实验分析
二氧化碳密度比空气大,倾倒时会在烧杯底部先聚积较多的二氧化碳,在下方蜡烛首先接触到较多的二氧化碳而先熄灭,上方的蜡烛后接触到二氧化碳而熄灭
5.实验结论
二氧化碳密度比空气大(物理性质)
二氧化碳不能燃烧也不支持燃烧(化学性质)
二、二氧化碳的溶解性实验
1.实验装置图
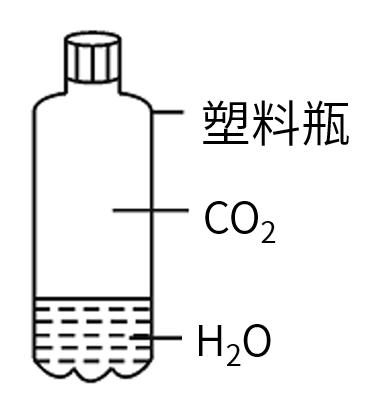
2.实验操作
向收集满二氧化碳气体的质地较软的塑料瓶中加入约1/3体积的水,立即旋紧瓶盖,振荡。观察现象并分析。
3.实验现象
塑料瓶变瘪(注意瘪的书写)
4.实验分析
部分二氧化碳溶于水,使瓶内气体减少,气压降低,在大气压的作用下将塑料瓶压瘪
5.实验结论
二氧化碳能溶于水
三、二氧化碳与水的反应
1.实验装置图
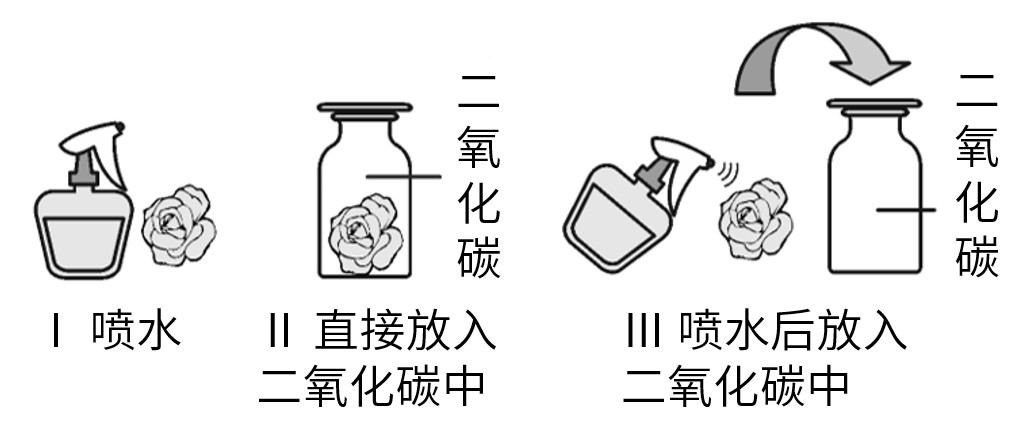
2.实验操作
取三朵用石蕊溶液染成紫色的干燥的纸花。第Ⅰ朵纸花喷上水,第Ⅱ朵纸花直接放入盛满二氧化碳的集气瓶中,第Ⅲ朵纸花喷上水后,再放入盛满二氧化碳的集气瓶中,观察三朵纸花的颜色变化。然后将第Ⅲ朵纸花取出,小心地用吹风机烘干,观察现象。
3.实验现象及分析
Ⅰ:纸花不变色
分析:水不能使纸花变色
Ⅱ:纸花不变色
分析:二氧化碳不能使纸花变色
Ⅲ:纸花由紫色变为红色
分析:二氧化碳与水反应生成新物质,使纸花变红
烘干第Ⅲ朵纸花:纸花由红色变为紫色
分析:碳酸不稳定,受热后易分解
4.实验结论
二氧化碳能与水反应生成碳酸,碳酸不稳定,受热易分解
5.注意
使纸花变色的,不是水,也不是二氧化碳,而是二氧化碳与水反应生成的碳酸
四、二氧化碳的性质归纳
1.物理性质
无色无味的气体
密度比空气大(可用向上排空气法收集)
能溶于水(不能用排水法收集)
2.化学性质
(1)不能燃烧,也不支持燃烧(用于灭火)
(2)二氧化碳能与水反应
(碳酸不稳定易分解)
(3)二氧化碳能使澄清石灰水变浑浊(用于检验二氧化碳)
(4)有些地方把碳与二氧化碳的反应也归纳进去了,建议放到碳的化学性质
一氧化碳还原氧化铜
一、装置图
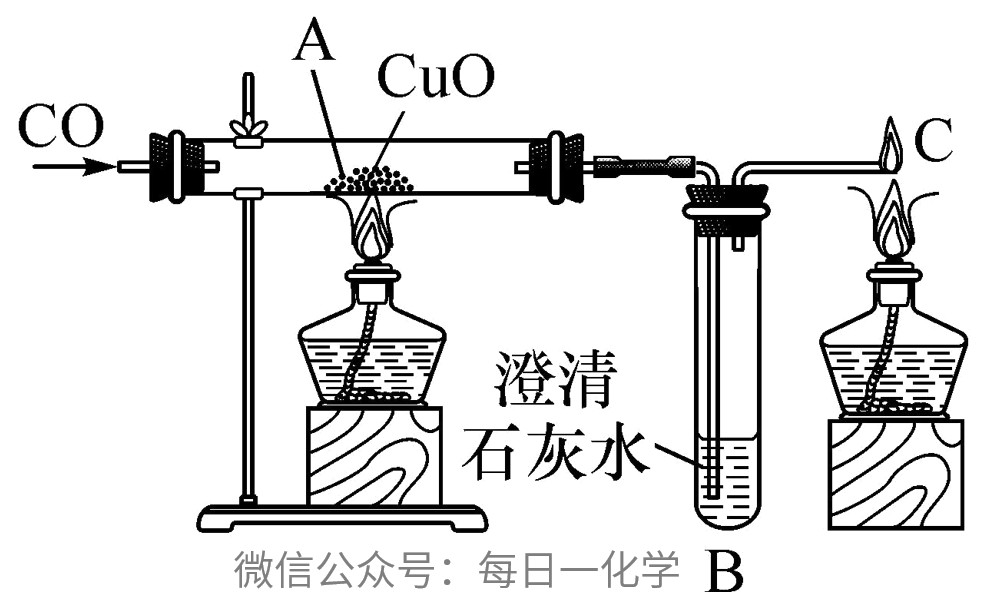
二、化学方程式
A处:
B处:
C处:
三、现象
A处:黑色粉末变为红色
B处:澄清石灰水变浑浊
C处:气体被点燃,火焰呈蓝色
四、注意事项
1.C处尾气处理的原因:CO有毒,防止污染空气(处理尾气,防止污染空气)
2.尾气处理的方式:点燃尾气;用气球收集
3.CO先来后走:实验开始时,先通CO,后点燃A处酒精灯;实验结束时,先熄灭A处酒精灯,后停止通入CO
4.CO先来的原因:排尽装置内的空气,防止混有CO的空气加热时发生爆炸
5.CO后走的原因:
(1)防止生成的铜重新被氧化
(2)防止液体倒吸,使玻璃管炸裂
解释:如果通CO那一端是开口,答案为防止生成的铜重新被氧化,如果是密封则应该是防止液体倒吸,使玻璃管炸裂,需根据具体情况回答